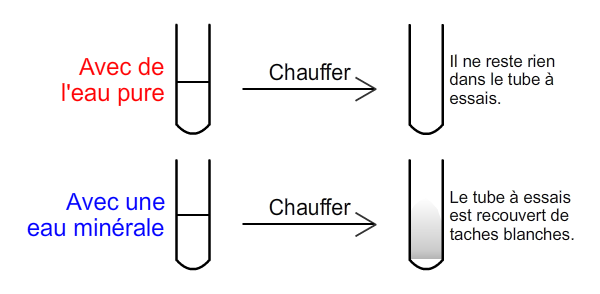
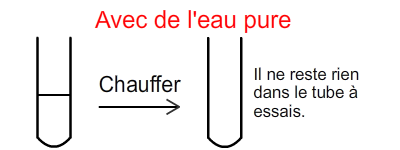
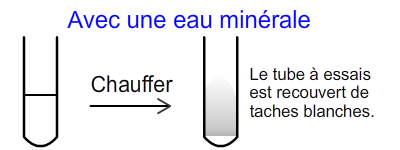
L'eau pure contient uniquement des molécules d'eau.
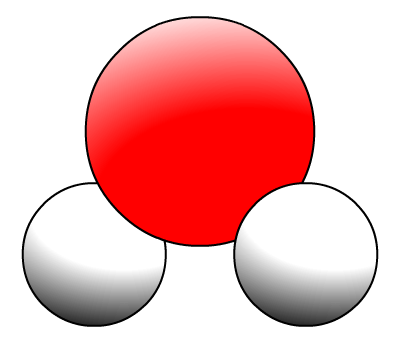
La molécule d'eau a pour formule H2O.
Elle comporte deux atomes d'hydrogène et un atome d'oxygène.
Son modèle est :
Les eaux minérales contiennent essentiellement des molécules d'eau et une faible proportion d'ions. Ces ions proviennent de la dissolution de sels comme le chlorure de sodium.
Par exemple, l'ion calcium qui a pour formule Ca2+.
La formule d'un ion comporte en exposant le signe + ou - et parfois un chiffre.
Exemples : Mg2+, SO42-, Cl-…
Reproduction de l'étiquette d'une eau minérale
Minéralisation moyenne en mg/L
| Calcium | Ca2+ | 176 |
| Magnésium | Mg2+ | 46 |
| Sodium | Na+ | 28 |
| Potassium | K+ | 5 |
| Sulfates | SO42- | 372 |
| Bicarbonates | HCO3- | 312 |
| Chlorures | Cl- | 37 |
| Fluor | F- | 1,3 |
| *Nitrates | NO3- | <0,5 |
Résidu sec à 180 oC : 859 mg/L
pH 7.2
Source du clos de l'abbaye.